Schema della sezione
-
LINK PER CONSULTARE IL CALENDARIO DIDATTICO PER IL SECONDO SEMESTRE:
https://unite.prod.up.cineca.it/calendarioPubblico/linkCalendarioId=68c42180bb495f00554c0834
-
-
-
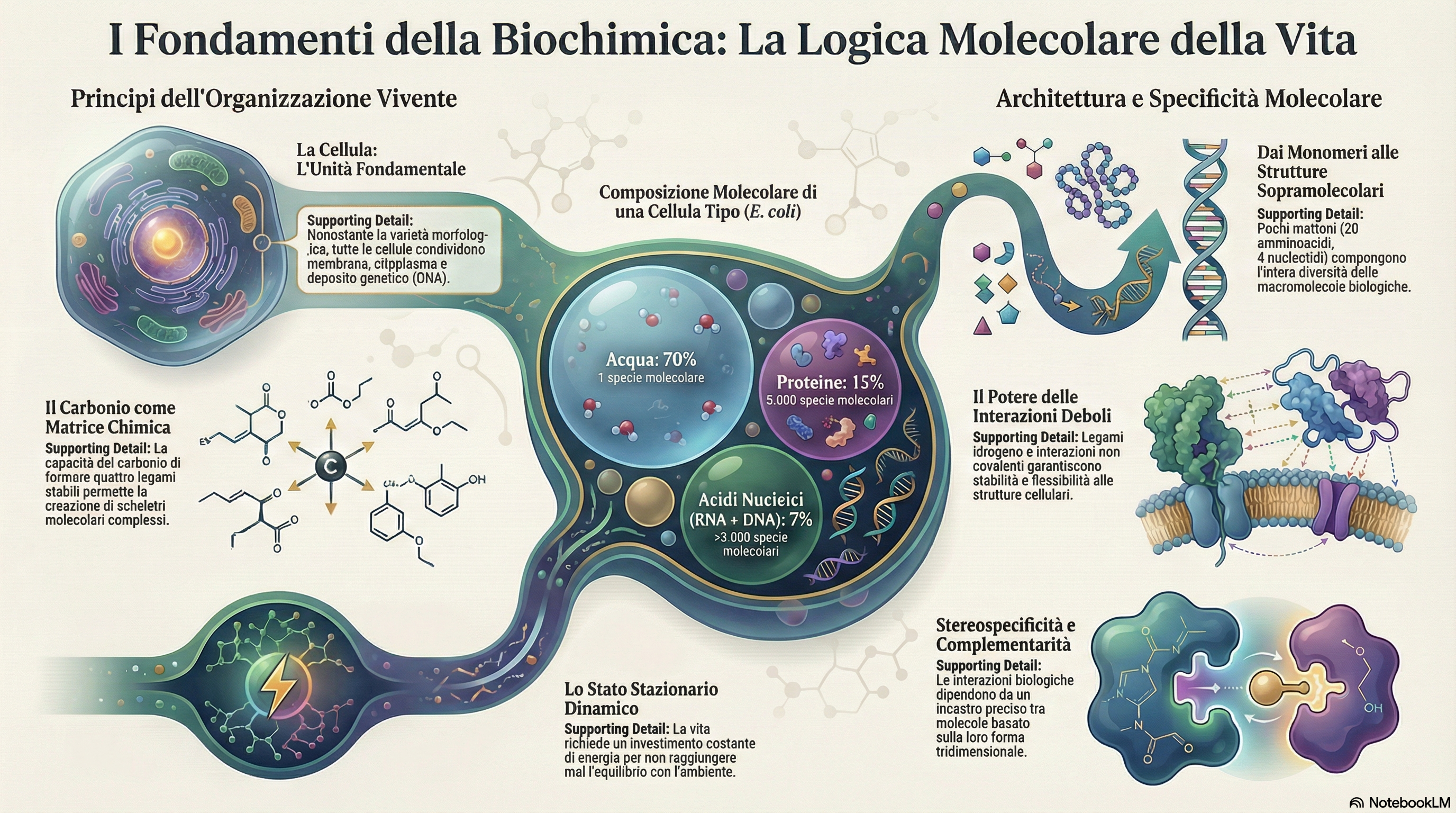
Riassunto Esecutivo: La Logica Molecolare della Vita
Circa quattordici miliardi di anni fa, l'universo ebbe inizio con un'emissione inimmaginabile di calore e particelle subatomiche. Attraverso eoni di espansione e raffreddamento, la gravità condensò la materia nelle prime stelle; le successive esplosioni di supernove fornirono l'energia necessaria per forgiare gli elementi complessi che oggi costituiscono i pianeti. Circa quattro miliardi di anni fa, sulla Terra, comparvero microrganismi capaci di estrarre energia per sintetizzare biomolecole. Tutti gli organismi viventi sono, letteralmente, "polvere di stelle".
La biochimica non è solo lo studio delle molecole della vita, ma la disciplina che si propone di decodificare la logica molecolare della vita: quell'insieme di principi organizzativi e leggi fondamentali che regolano l'interazione tra migliaia di molecole inanimate. Se isolate, queste molecole seguono le medesime leggi chimico-fisiche della materia non vivente; tuttavia, quando integrate, esse operano in modo coordinato per mantenere, riprodurre e perpetuare lo stato vivente.
Messaggi chiave del capitolo:
- Unità nelle Leggi, Specificità nell'Ordine: La vita non viola le leggi della fisica, ma le sfrutta attraverso un'organizzazione microscopica di altissima complessità.
- Il Vincolo della Diffusione: La struttura cellulare è limitata da parametri fisici invalicabili, come il rapporto superficie-volume, che determina le dimensioni ottimali per la sopravvivenza.
- Sinergia tra Evoluzione e Metabolismo: La biodiversità, suddivisa in tre domini, emerge da strategie metaboliche differenziate per l'acquisizione di energia e carbonio.
Questa profonda unità biochimica è il punto di partenza per comprendere come le proprietà macroscopiche degli organismi emergano dal mondo molecolare.
-
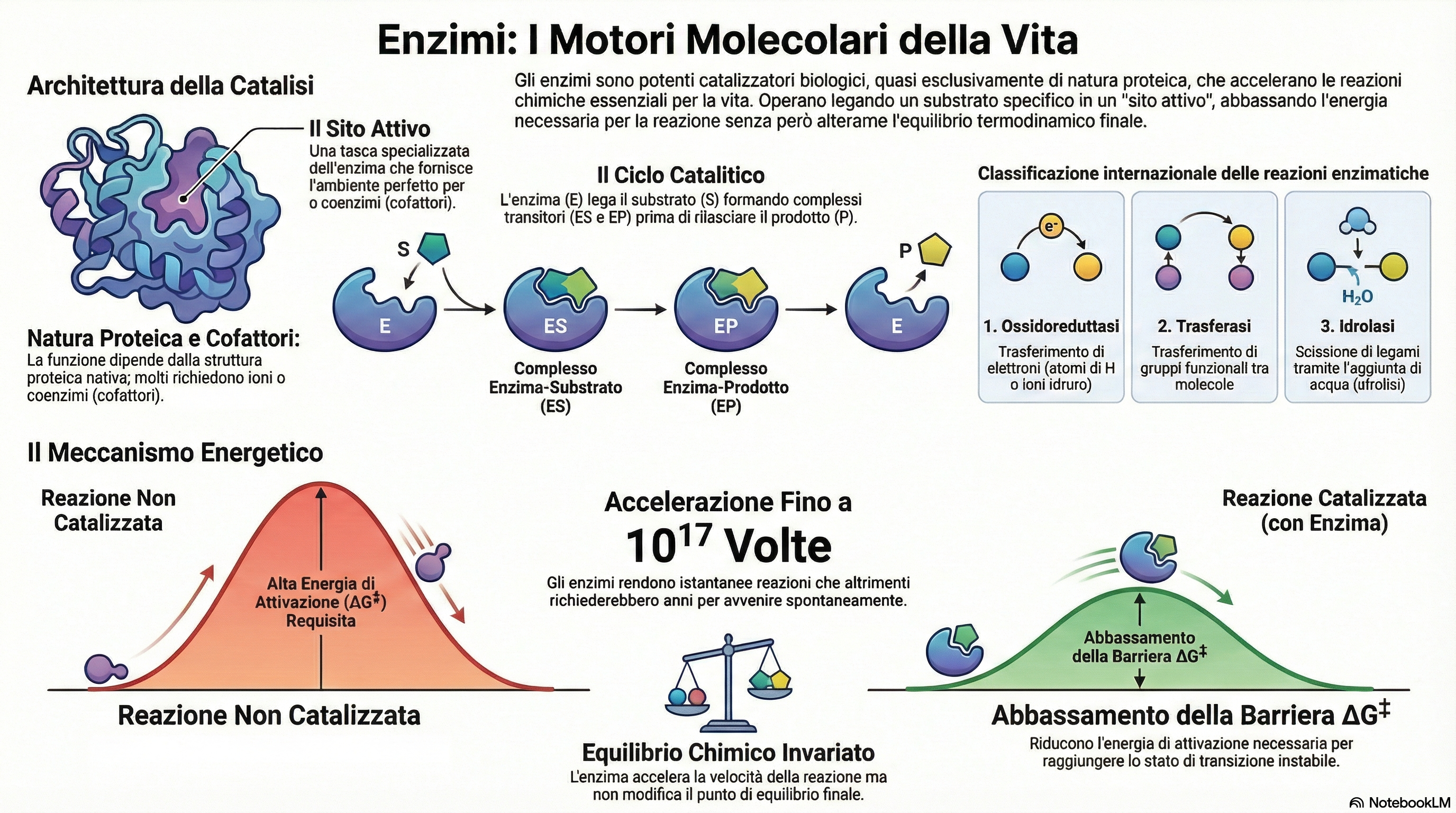
Riassunto EsecutivoLa vita biologica si fonda su due prerequisiti essenziali: l’autoreplicazione e la catalisi. Gli enzimi, proteine altamente specializzate, rappresentano i motori molecolari di quest'ultima, dotati di un potere catalitico e di una selettività che superano di gran lunga qualsiasi catalizzatore inorganico o sintetico. Il loro ruolo non è quello di rendere possibili reazioni "impossibili", bensì quello di accelerare processi che, pur essendo termodinamicamente favoriti, risulterebbero cineticamente trascurabili.
Un esempio emblematico è offerto dal saccarosio. La sua conversione in CO2 e H2O è un processo altamente esoergonico (ΔG'° negativo), capace di rilasciare l'energia necessaria alle funzioni vitali. Tuttavia, in assenza di catalisi, una bustina di zucchero rimane inerte per anni poiché la barriera energetica per la sua degradazione è estremamente elevata. All'interno di un organismo, grazie agli enzimi, questa stessa reazione avviene in pochi secondi. Gli enzimi operano dunque abbassando le barriere di attivazione, permettendo alla cellula di trasformare l'energia chimica in tempi biologicamente utili.
Il valore della comprensione ("So What?"): Senza l'azione enzimatica, il metabolismo umano si fermerebbe istantaneamente. Alla temperatura corporea e a pH neutro, le biomolecole sono intrinsecamente stabili; le barriere energetiche necessarie per rompere o formare legami chimici risulterebbero insormontabili, rendendo la vita, intesa come flusso dinamico di materia ed energia, fisicamente irrealizzabile.
VIDEO -
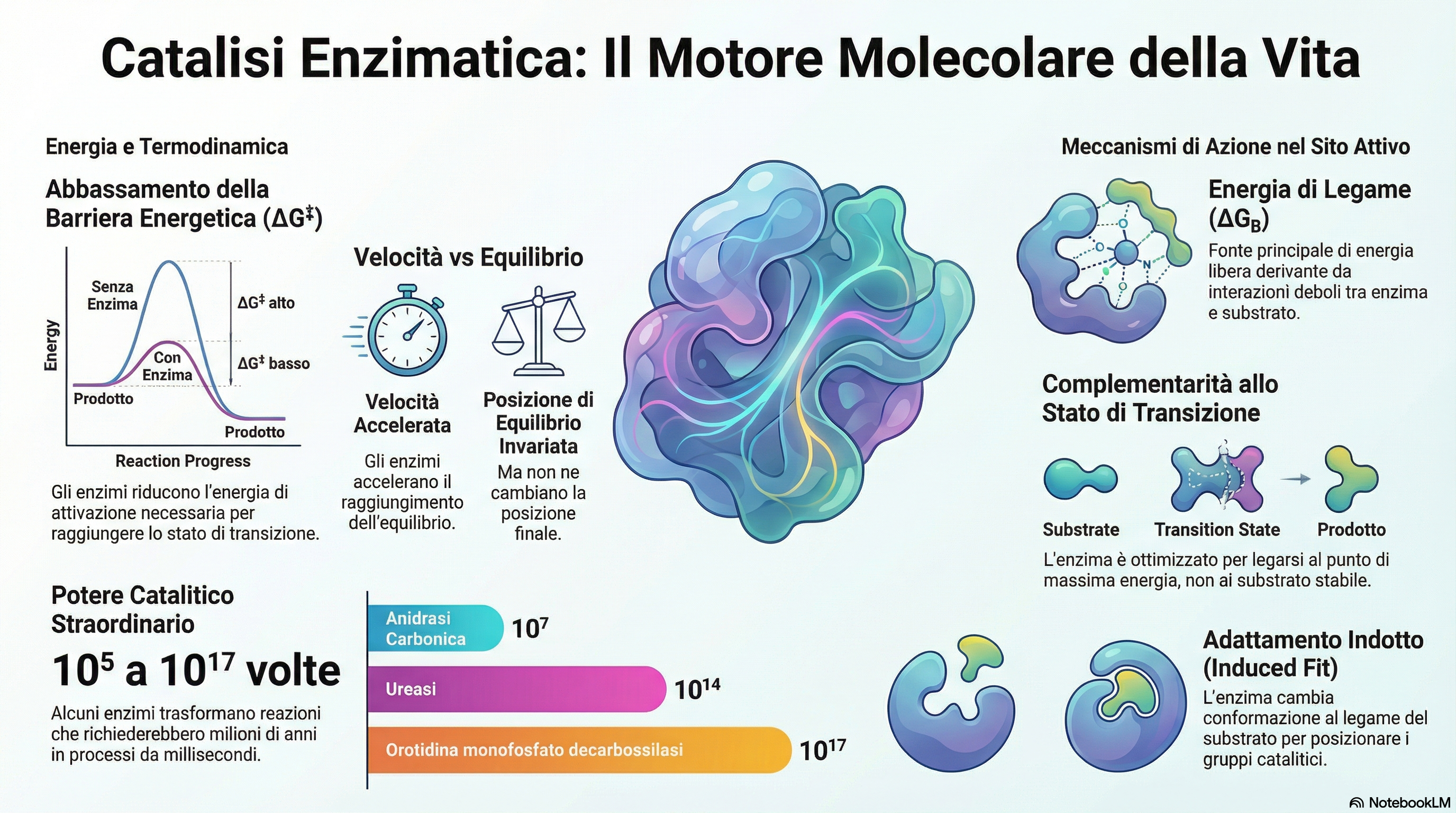
Riassunto Esecutivo: Catalisi enzimatica
Se dovessimo individuare i "registi" occulti che orchestrano ogni singola operazione nel metabolismo animale, non avremmo dubbi: sono gli enzimi. Senza la loro incessante attività, la vita non sarebbe altro che un concetto teorico, poiché le reazioni chimiche necessarie per sostenere un organismo avverrebbero con una lentezza incompatibile con l'esistenza. Possiamo definire gli enzimi come catalizzatori di natura proteica straordinariamente efficienti. Essi permettono alla cellula di operare in condizioni "gentili" — temperature fisiologiche e pH neutro — trasformando processi che richiederebbero milioni di anni in eventi che si consumano in millisecondi.
I messaggi chiave che guideranno il nostro studio sono tre:
- Efficienza e Riciclo: Gli enzimi accelerano le reazioni da 105 a 1017 volte senza essere consumati. Ogni enzima emerge dal ciclo catalitico intatto, pronto per una nuova sfida.
- Abbassamento delle Barriere: Non modificano la natura chimica della reazione, ma abbassano la "collina energetica" (energia di attivazione) che i reagenti devono scalare.
- Neutralità Termodinamica: Un enzima non può far avvenire una reazione impossibile. Esso non tocca l'equilibrio finale, ma accelera semplicemente il tempo necessario per raggiungerlo.
Perché è importante? Considerate che la decarbossilazione dell'orotidina monofosfato richiederebbe 78 milioni di anni in assenza di catalisi; grazie al suo enzima, avviene in millisecondi. Comprendere questa potenza richiede di analizzare la logica molecolare della loro struttura: il sito attivo.
VIDEO -
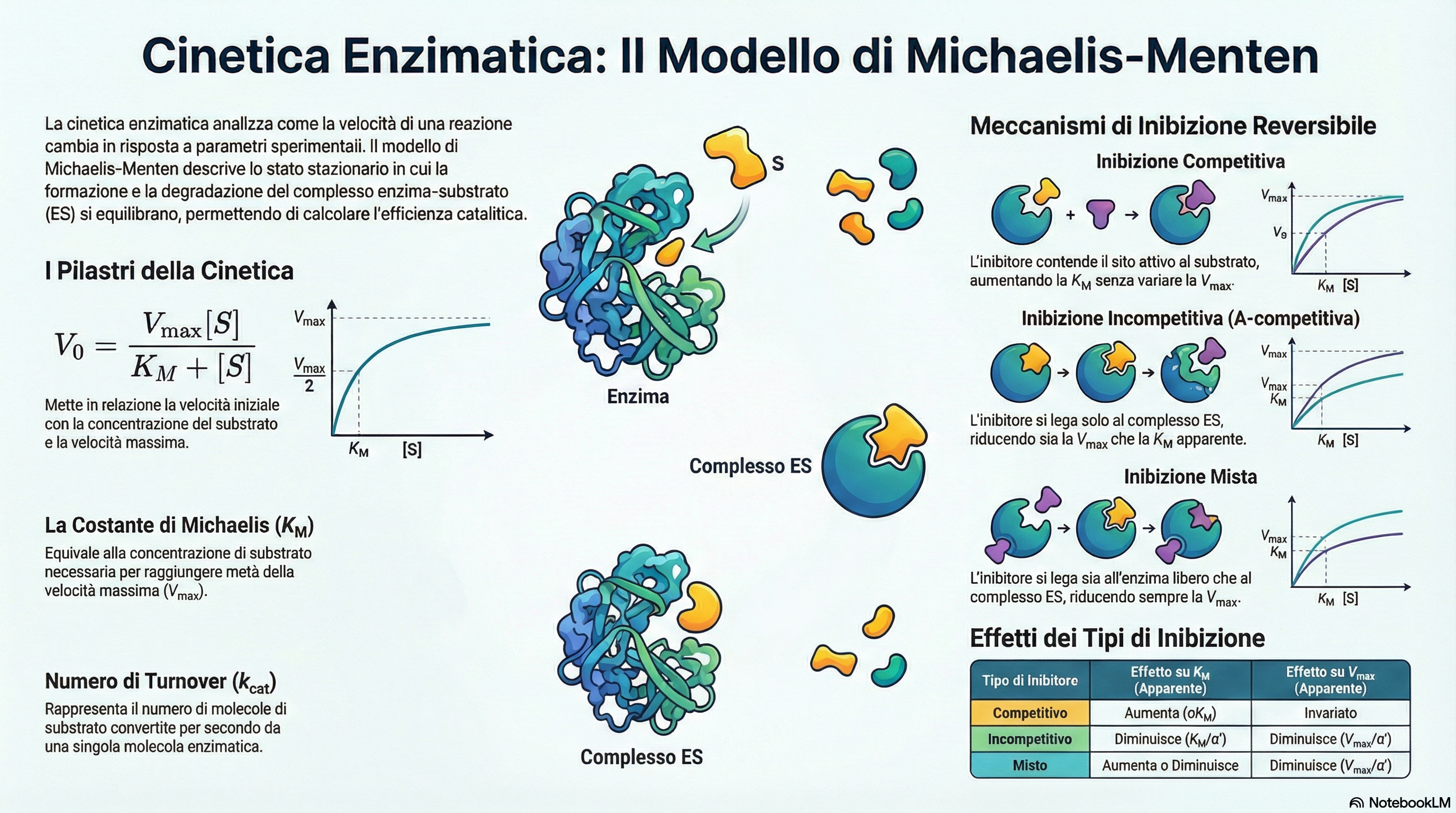
1. Riassunto Esecutivo: Cinetica enzimatica
La cinetica enzimatica è la disciplina quantitativa che decifra il meccanismo d'azione degli enzimi attraverso la determinazione della velocità di reazione e della sua variazione in risposta a parametri sperimentali. Più che una semplice branca della chimica fisica, essa rappresenta lo strumento fondamentale per trasformare la biologia da una scienza puramente descrittiva a una disciplina predittiva. Comprendere la cinetica significa essere in grado di calcolare non solo se una reazione avverrà, ma con quale rapidità essa sosterrà la vita cellulare o risponderà a un intervento farmacologico.
Il modello di Michaelis-Menten costituisce la pietra angolare di questa analisi. Attraverso i parametri cardine Km (costante di Michaelis) e Vmax (velocità massima), è possibile definire l'identità funzionale di un enzima. Mentre la Vmax riflette la capacità catalitica estrema alla saturazione, la Km indica la concentrazione di substrato necessaria per un'attività significativa, riflettendo spesso l'adattamento evolutivo dell'enzima al suo ambiente cellulare. L'analisi quantitativa della catalisi permette di distinguere la specificità enzimatica dalla catalisi chimica semplice, fornendo la base per il rational drug design. Per padroneggiare queste equazioni, tuttavia, è essenziale comprendere i presupposti fisici della derivazione, a partire dalla distinzione tra gli stati temporali della reazione.
VIDEO -
1. Riassunto Esecutivo
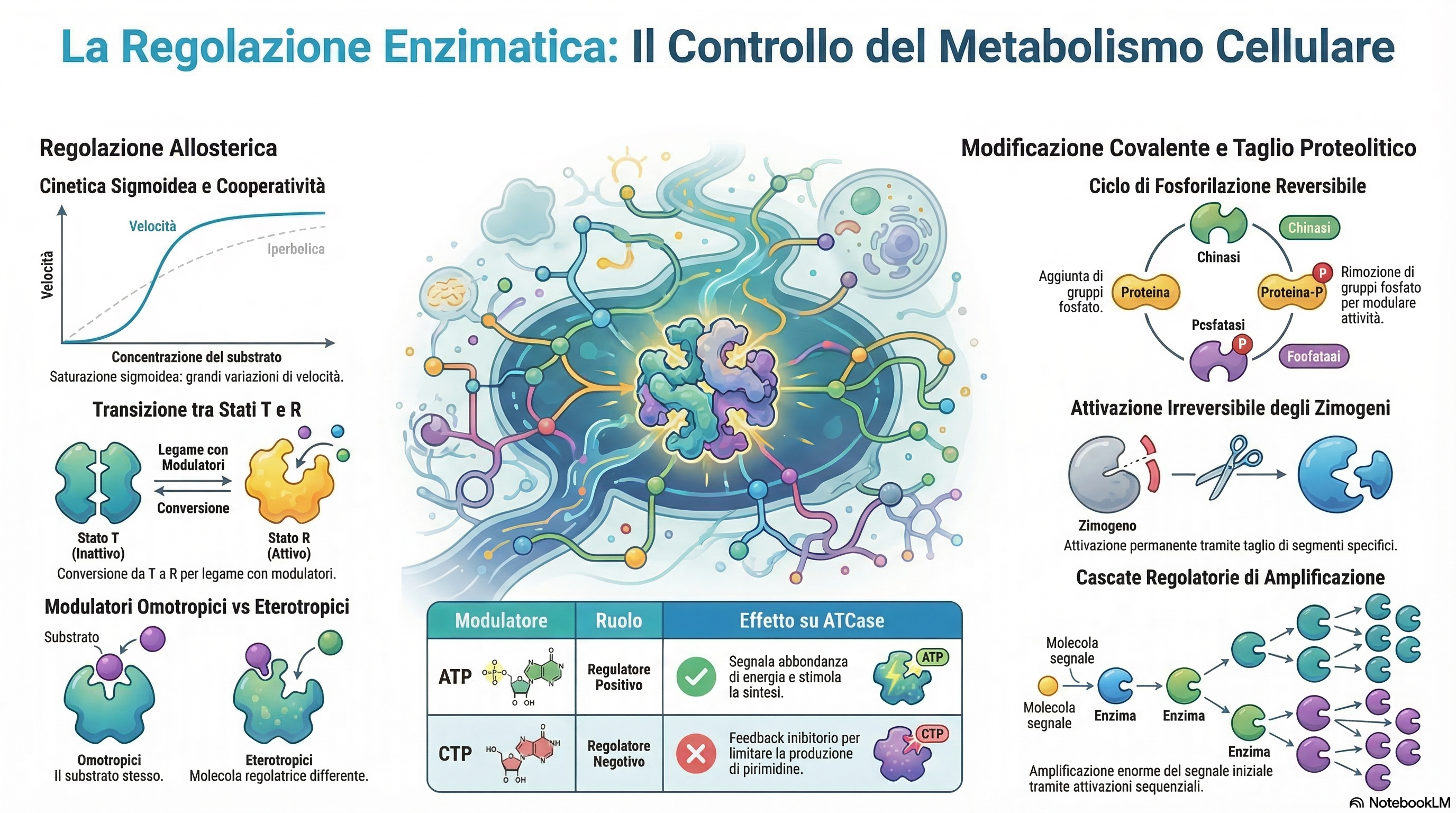
All'interno dell'ambiente cellulare, il metabolismo non deve essere interpretato come un insieme caotico di reazioni indipendenti, ma come un sistema magistralmente orchestrato. In questa "sinfonia" molecolare, gli enzimi regolatori fungono da centri di controllo strategici o "checkpoint". Una cellula, infatti, non catalizza tutte le reazioni possibili simultaneamente; al contrario, essa modula l'attività enzimatica per rispondere con precisione millimetrica alle mutevoli esigenze di energia e biomolecole. Se ogni reazione procedesse alla massima velocità senza controllo, le macromolecole verrebbero rapidamente degradate in forme chimiche troppo semplici, portando al collasso del sistema.
L'efficienza energetica e la sopravvivenza dell'organismo dipendono dalla capacità di questi enzimi di modulare la propria velocità catalitica in risposta a segnali specifici. Esistono quattro meccanismi principali di regolazione:
- Allosterismo: basato sul legame non covalente e reversibile di modulatori che inducono cambiamenti conformazionali.
- Modificazioni covalenti reversibili: come l'aggiunta di gruppi chimici (es. fosforilazione) che alterano le proprietà degli aminoacidi.
- Proteine regolatrici: proteine la cui unica funzione è interagire non covalentemente con un enzima per modularne l'attività.
- Scissione proteolitica: un meccanismo irreversibile che attiva precursori latenti (zimogeni).
In questa lezione analizzeremo come la cellula gestisca le proprie risorse in modo economico e intelligente, trasformando una serie di passaggi biochimici in un processo vitale coordinato. Comprendere questi meccanismi è essenziale non solo per la biochimica pura, ma per la pratica clinica veterinaria, poiché essi governano l'omeostasi e rappresentano il bersaglio di interventi farmacologici cruciali.
VIDEO -
1. Riassunto Esecutivo
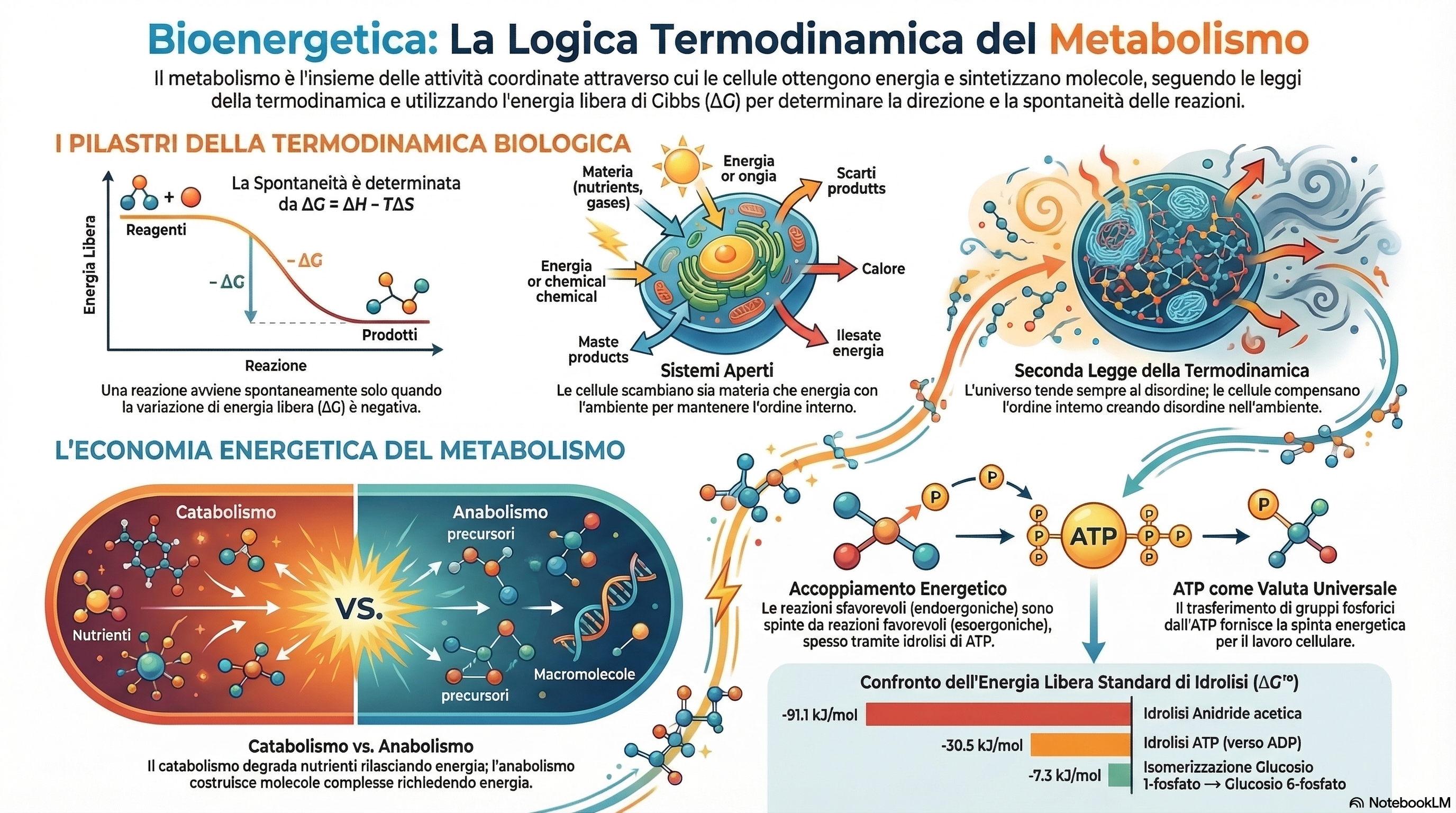
Il metabolismo non è una sterile sequenza di nomi, ma la logica operativa che permette a un organismo animale di "restare in vita". Esso rappresenta l'insieme coordinato delle attività cellulari attraverso cui i precursori vengono convertiti in prodotti tramite una serie di intermedi chiamati metaboliti. L'insieme di queste vie che interconvertono precursori e prodotti a basso peso molecolare è definito metabolismo intermedio.
Il metabolismo si regge sull'equilibrio tra due fasi strategiche: il catabolismo, la fase degradativa che estrae energia dai nutrienti (carboidrati, grassi, proteine), e l'anabolismo (o biosintesi), la fase costruttiva che richiede energia per formare macromolecole complesse (proteine, lipidi di membrana, acidi nucleici). In questa dinamica, l'ATP (adenosina trifosfato) agisce come la "valuta energetica" universale, mediando il trasferimento di energia dai processi che la rilasciano a quelli che la consumano.
Queste trasformazioni non sono casuali, ma seguono rigorosamente le leggi della termodinamica, che determinano la spontaneità delle reazioni. Tuttavia, non lasciatevi spaventare dalla complessità: la natura opera secondo un principio di economia evolutiva. Migliaia di reazioni biochimiche apparentemente diverse possono essere ridotte a sole cinque classi fondamentali. Imparare questi pattern vi permetterà di decifrare qualsiasi pathway metabolico incontrerete nella vostra pratica clinica.
Per comprendere questa armonia molecolare, dobbiamo prima analizzare i principi fisici che governano il "budget energetico" della cellula.
VIDEO -
1. Riassunto Esecutivo
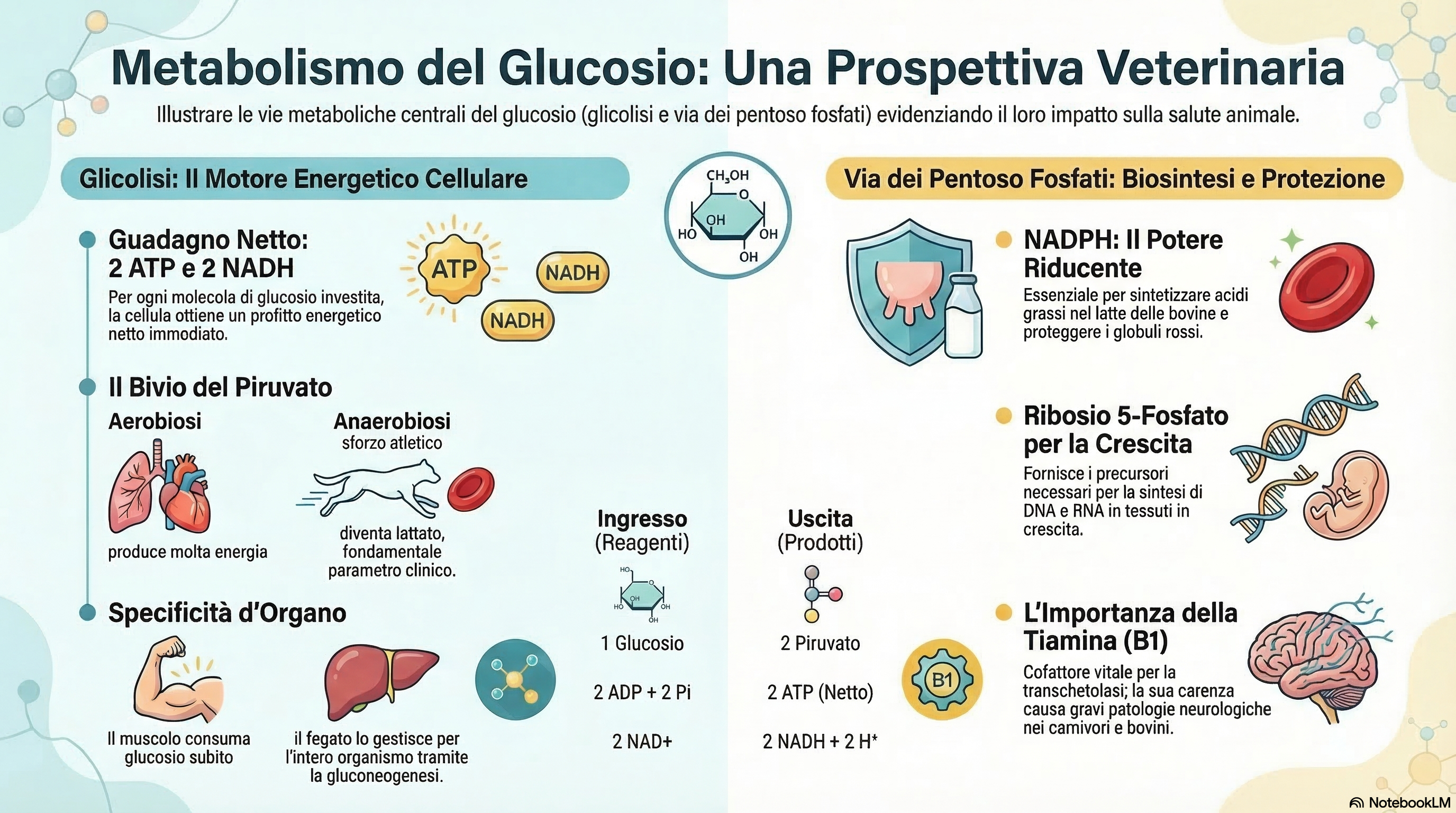
Il glucosio non è semplicemente un nutriente; è il crocevia metabolico universale, una molecola la cui versatilità sostiene la vita animale. Per un futuro medico veterinario, la padronanza delle tre vie principali che governano il glucosio — glicolisi, gluconeogenesi e via del pentosio fosfato (PPP) — è un requisito clinico imprescindibile. Queste vie non producono solo la “valuta energetica” della cellula (), ma forniscono anche il “potere riducente” ( e ) e i mattoni strutturali (ribosio) necessari per la sintesi di e .
È imperativo comprendere che l’alterazione di questi flussi biochimici si traduce direttamente in quadri patologici gravi. Un cucciolo in crisi ipoglicemica per parvovirosi, un gatto in chetoacidosi diabetica o un cavallo atleta in acidosi lattica non sono altro che manifestazioni cliniche di squilibri in queste reazioni. Come vedremo, la logica molecolare che regola il destino del glucosio è ciò che permette ai tessuti glucosio-dipendenti, come i globuli rossi e la retina, di sopravvivere anche in condizioni di stress estremo.
Il glucosio si presenta dunque come una molecola dinamica, pronta a rispondere alle diverse esigenze fisiologiche attraverso quattro rotte strategiche ben definite.
-
1. Riassunto Esecutivo
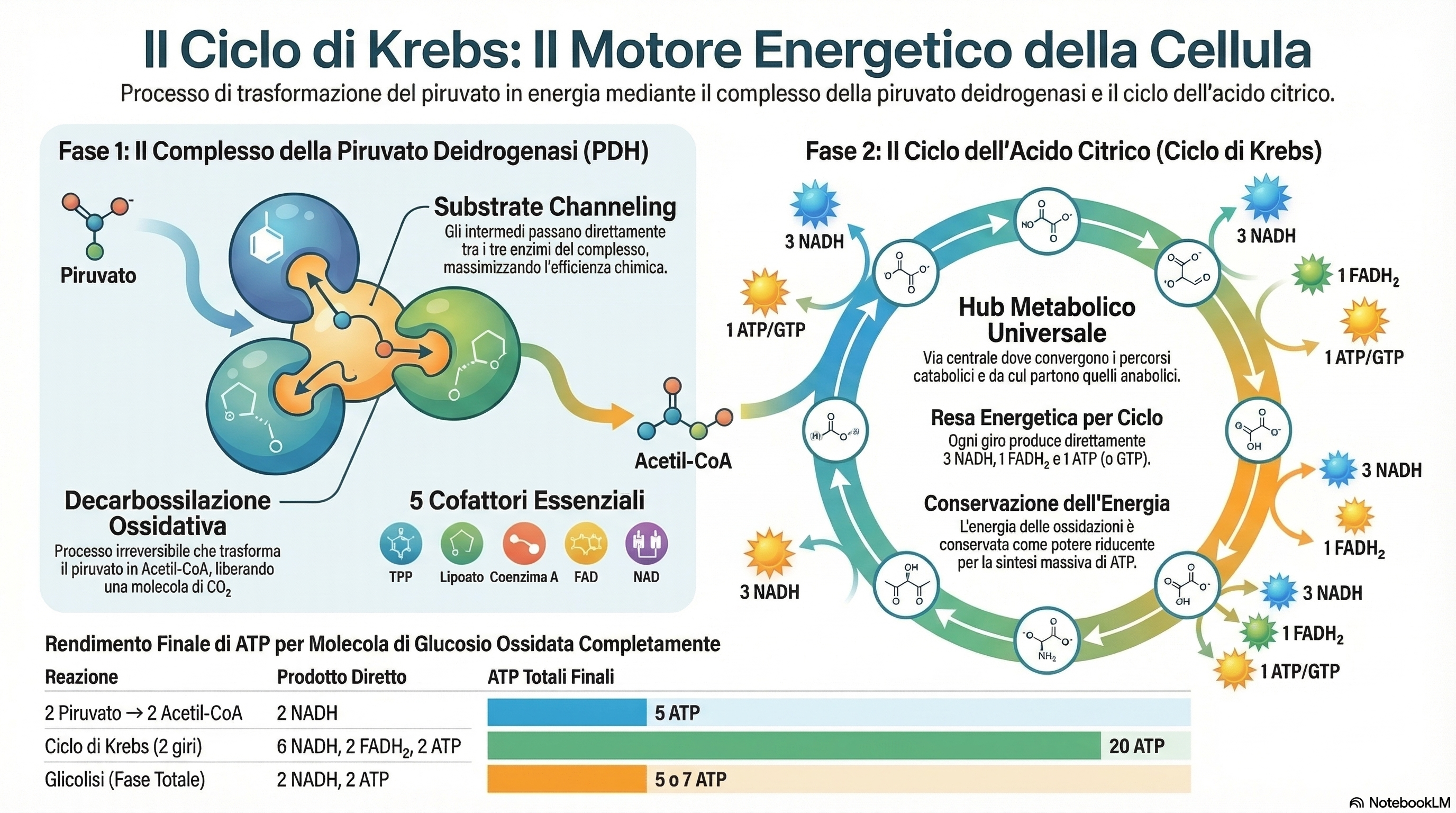
Il Ciclo di Krebs, noto anche come ciclo dell’acido citrico o ciclo degli acidi tricarbossilici (TCA), rappresenta il cuore pulsante del metabolismo energetico cellulare. In termini biochimici, esso costituisce la seconda fase della respirazione cellulare, il processo mediante il quale il piruvato derivante dalla glicolisi viene ulteriormente ossidato ad acqua () e anidride carbonica ().
Per uno studente di medicina veterinaria, comprendere questo ciclo significa padroneggiare la logica con cui l’organismo animale estrae energia dai nutrienti assorbiti attraverso il tratto intestinale. Il punto di ingresso fondamentale è l’Acetil-CoA (Acetato attivato), una molecola che convoglia i prodotti della degradazione di carboidrati, grassi e amminoacidi verso un’ossidazione completa. Tuttavia, il Ciclo di Krebs non deve essere visto solo come una via degradativa (catabolica); esso agisce come un vero e proprio “hub” metabolico, fornendo intermedi necessari per la sintesi di amminoacidi, acidi grassi e steroli (anabolismo). Questa doppia natura lo rende una via anfibolica essenziale per l’omeostasi e l’efficienza biologica di ogni specie animale.
-
1. Riassunto Esecutivo
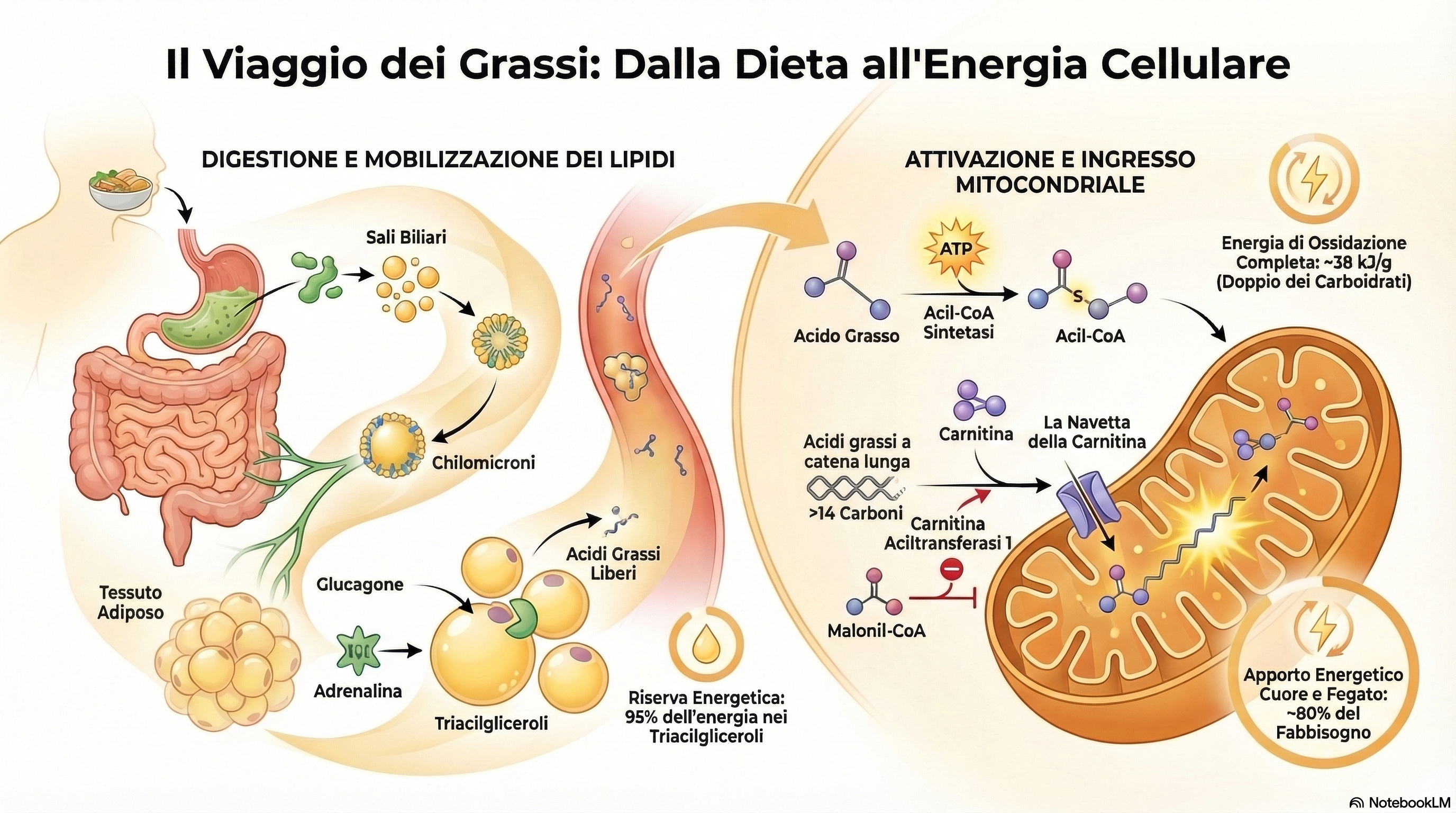
Il catabolismo degli acidi grassi rappresenta una via metabolica d’elezione per la produzione di energia, fondamentale per l’omeostasi dei vertebrati. In tessuti ad alta intensità di lavoro come il cuore e il fegato dei mammiferi, l’ossidazione degli acidi grassi fornisce circa l’80% del fabbisogno energetico totale. Questa efficienza non è limitata ai mammiferi: basti pensare agli uccelli migratori o agli animali in letargo, che dipendono quasi esclusivamente dai grassi per sostenere sforzi prolungati o lunghi periodi di digiuno.
Il messaggio chiave di questo modulo è la trasformazione di molecole inerti e insolubili in energia pronta all’uso (ATP). Questo avviene attraverso la -ossidazione, un processo mitocondriale che smantella le catene idrocarburiche in unità di Acetil-CoA. Come vedremo, la sfida biochimica risiede nel superare l’insolubilità dei lipidi nei liquidi biologici e la stabilità dei legami carbonio-carbonio. Attraverso una serie di tappe coordinate — digestione, mobilizzazione ormonale, attivazione e trasporto mediante il sistema della carnitina — la cellula riesce a convogliare questi substrati nel ciclo dell’acido citrico e nella catena respiratoria.
-
1. Riassunto Esecutivo
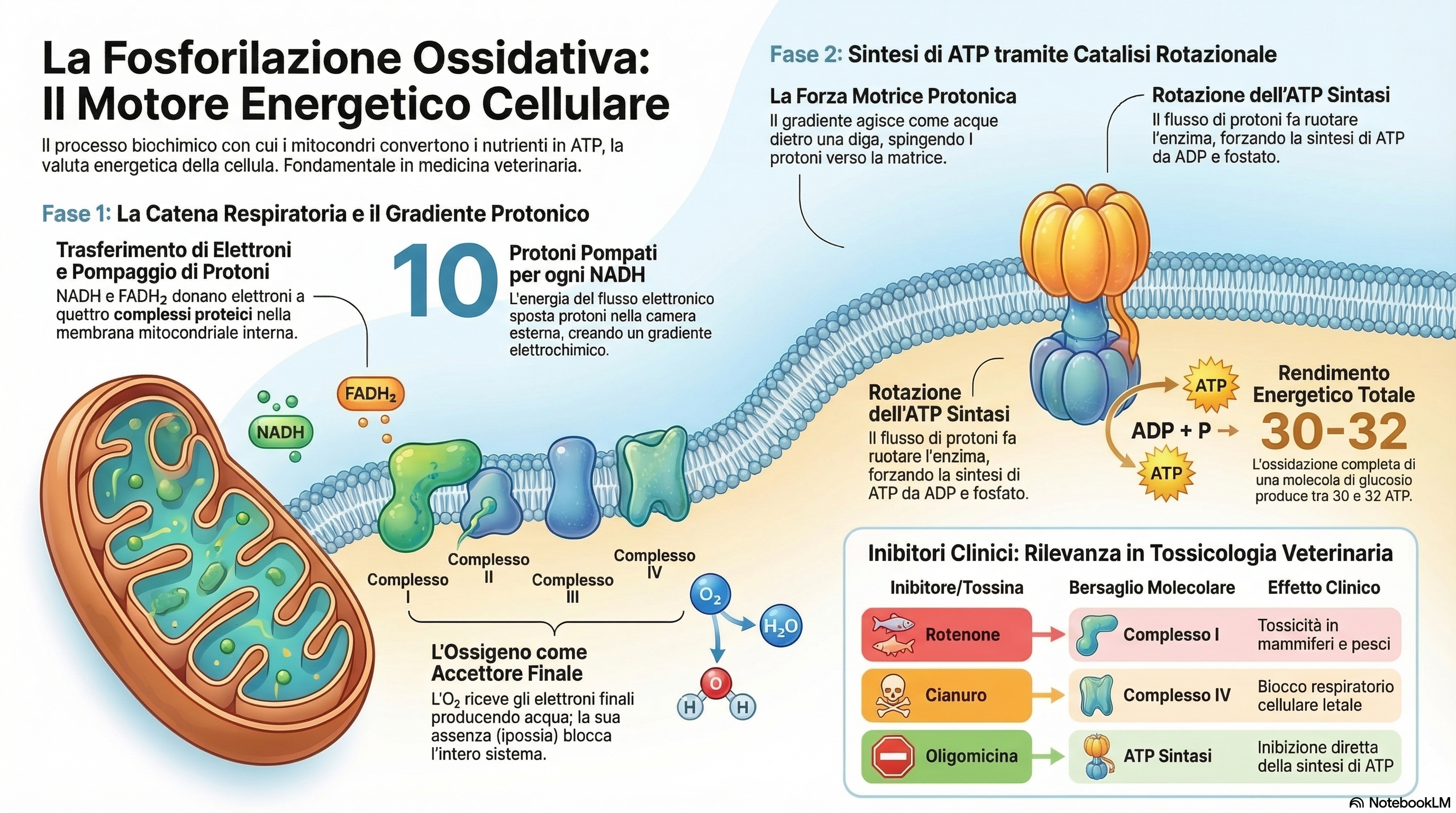
La fosforilazione ossidativa rappresenta l’apice della bioenergetica cellulare, il processo molecolare mediante il quale l’energia derivante dall’ossidazione dei nutrienti viene trasdotta in adenosina trifosfato (ATP). All’interno dei mitocondri, veri “hub” metabolici, l’energia chimica dei coenzimi ridotti (NADH e ) non viene convertita direttamente in ATP, ma trasformata inizialmente in un gradiente elettrochimico transmembrana.
Per visualizzare questo concetto, utilizziamo l’analogia della diga: i complessi della catena respiratoria agiscono come pompe che accumulano protoni nello spazio intermembrana (il bacino idrico). La forza motrice protonica risultante possiede due componenti distinte: una chimica (, l’alcalinità della matrice) e una elettrica (, il potenziale negativo interno). Il flusso di ritorno dei protoni attraverso la “turbina” dell’ATP sintasi permette la sintesi del legame fosfoanidridico.
L’ossigeno molecolare è l’accettore finale di questo flusso; la sua assenza (ipossia) o l’interferenza con i trasportatori causano un rapido collasso energetico. In medicina veterinaria, i tessuti ad alto metabolismo, come il miocardio e il sistema nervoso, sono i primi a subire danni irreversibili in condizioni di ipossia o tossicosi mitocondriale.
-
-
-
-
-
1. Riassunto Esecutivo
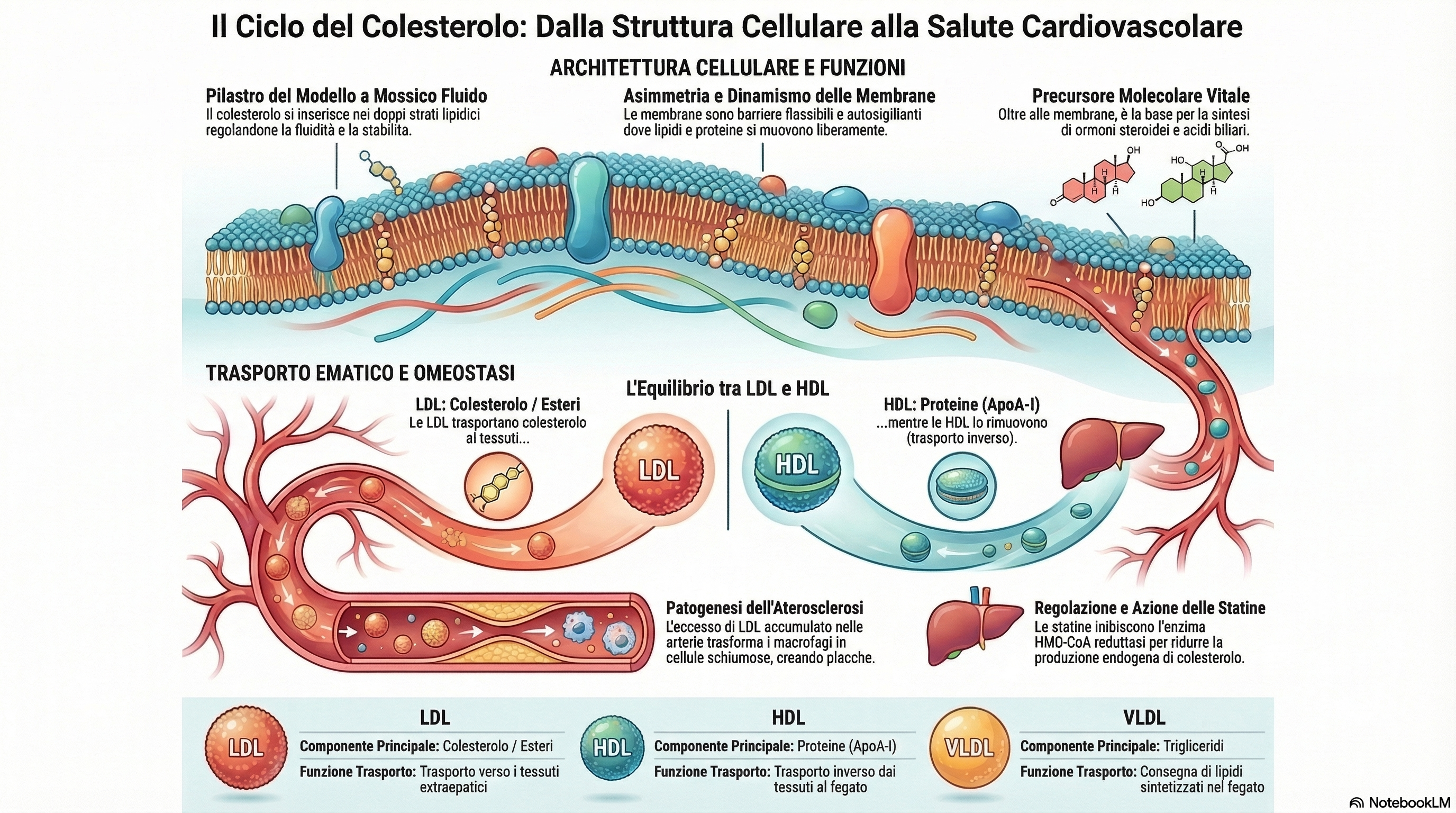
I lipidi rappresentano una classe di biomolecole essenziali non solo per il deposito energetico, ma per la definizione stessa dell’architettura cellulare. Le membrane biologiche, strutture dinamiche e complesse, segregano i processi biochimici e permettono la compartimentalizzazione necessaria alla vita eucariotica. Il modello del “mosaico fluido” descrive queste membrane come un doppio strato di lipidi polari che ospita proteine integrali e periferiche, garantendo una fluidità bidimensionale che facilita le interazioni molecolari.
In questo contesto, il colesterolo emerge come un modulatore cruciale della rigidità strutturale e come precursore biosintetico di molecole bioattive, tra cui ormoni steroidei, acidi biliari e vitamina D. Data la loro natura idrofobica, il trasporto sistemico dei lipidi avviene tramite le lipoproteine plasmatiche. Chilomicroni, VLDL, LDL e HDL coordinano il traffico di triacilgliceroli (TAG) e steroli tra l’intestino, il fegato e i tessuti periferici.
L’omeostasi del colesterolo è mantenuta da una rete di regolazione sofisticata che include il controllo trascrizionale via SREBP e sensori metabolici come i recettori LXR. Comprendere questi meccanismi è fondamentale nella medicina veterinaria e umana, poiché le disfunzioni nel metabolismo lipidico portano alla patogenesi dell’aterosclerosi. In tale patologia, l’accumulo di LDL ossidate nella matrice extracellulare delle pareti arteriose innesca una risposta infiammatoria che porta alla formazione della placca. La conoscenza di queste vie biochimiche permette l’uso razionale di interventi farmacologici, come le statine, che mirano all’inibizione della sintesi endogena per stimolare la clearance del colesterolo circolante.
-
1. Riassunto Esecutivo
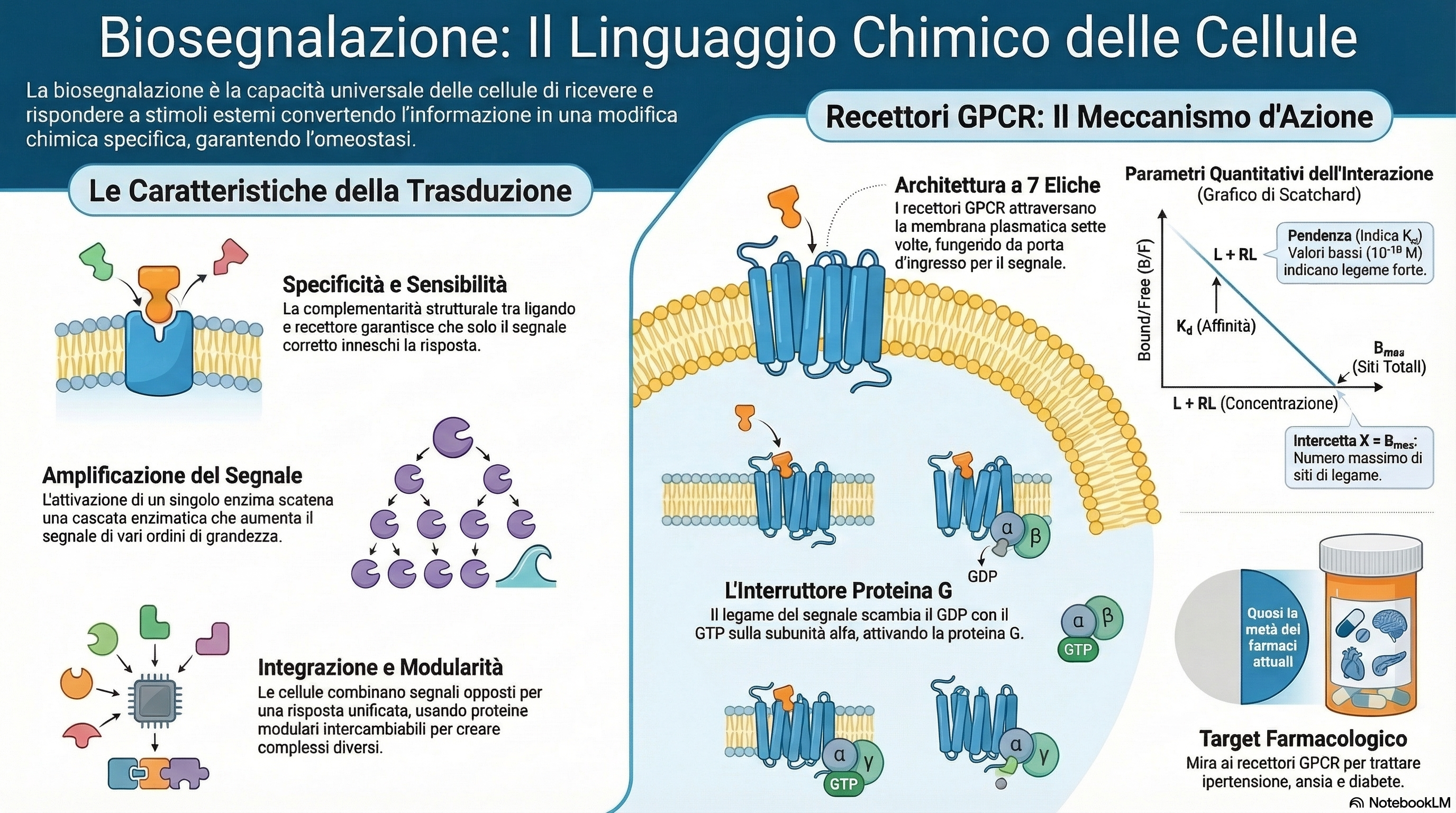
La biosegnalazione è il processo vitale mediante il quale le cellule percepiscono stimoli provenienti dall’ambiente extracellulare e li convertono in risposte biologiche specifiche. Questo fenomeno è tecnicamente definito trasduzione del segnale: l’informazione esterna non entra fisicamente nella cellula, ma viene “tradotta” in un cambiamento biochimico interno.
Tale capacità rappresenta una proprietà universale della vita, essenziale per la sopravvivenza a ogni livello di complessità biologica. Nei batteri, i recettori di membrana monitorano costantemente parametri quali il pH, la forza osmotica e la disponibilità di nutrienti, innescando risposte adattative come il movimento chemotattico o la formazione di spore. Negli organismi multicellulari, la biosegnalazione coordina l’attività di tessuti distanti attraverso lo scambio di ormoni e neurotrasmettitori, regolando l’omeostasi, la crescita e lo sviluppo embrionale. In sintesi, la trasduzione del segnale è il linguaggio molecolare che permette alla cellula di interpretare il mondo circostante e di rispondere in modo coerente alle sue variazioni.
-
1. Riassunto Esecutivo
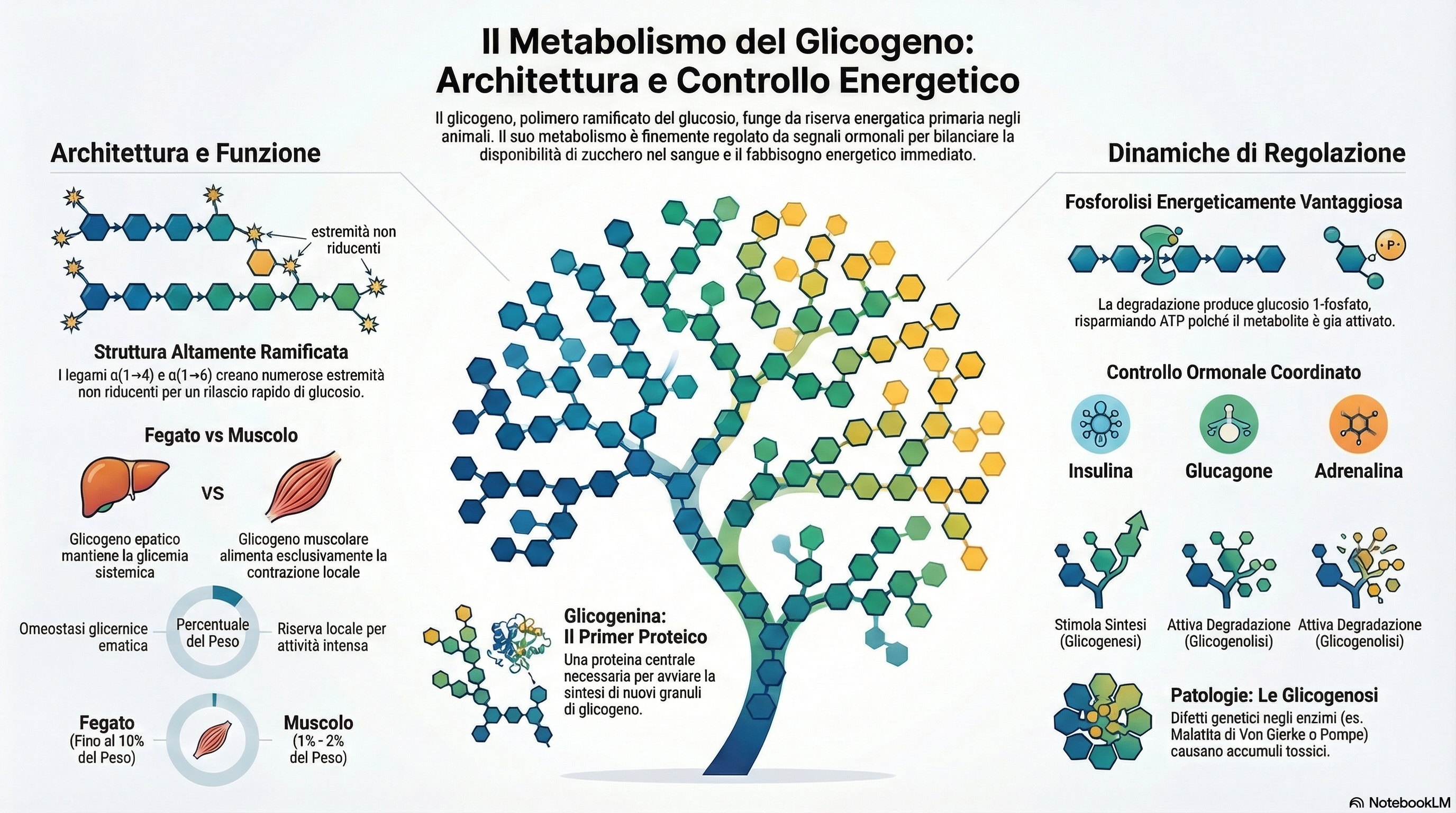
Il glicogeno è un polimero del glucosio che rappresenta la principale riserva energetica a rapida disponibilità per gli animali vertebrati. Sebbene l’organismo immagazzini circa cento volte più energia sotto forma di grassi (trigliceridi), il glicogeno ricopre un ruolo vitale e insostituibile: nei mammiferi, infatti, non esiste una via biochimica capace di convertire gli acidi grassi in glucosio. Di conseguenza, il glicogeno è l’unica “polizza assicurativa” immediata per organi glucosio-dipendenti come il cervello e per sostenere la contrazione muscolare intensa.
La logica fisiologica del glicogeno si divide tra due distretti principali: il fegato, che lo utilizza come serbatoio per mantenere costante la glicemia sistemica (omeostasi), e il muscolo scheletrico, che lo riserva egoisticamente per il proprio metabolismo energetico locale.
Dal punto di vista chimico, la sua struttura altamente ramificata risponde a due necessità cruciali: 1. Vantaggio Osmotico: Se il glucosio fosse libero nel citosol, la sua concentrazione renderebbe la cellula ipertonica, richiamando acqua fino alla rottura (lisi). Immagazzinarlo come una singola macromolecola riduce drasticamente l’osmolarità. 2. Efficienza enzimatica: La ramificazione moltiplica le “estremità non riducenti”, ovvero i punti di attacco per gli enzimi. Ciò consente una mobilizzazione del glucosio quasi istantanea, fondamentale nella risposta “combatti o fuggi”.
Il sistema è governato da una regolazione reciproca, mediata da ormoni e segnali allosterici (meccanismi in cui il legame di una molecola in un sito specifico dell’enzima ne altera l’attività). Questo assicura che sintesi e degradazione non avvengano mai contemporaneamente, evitando un inutile dispendio di energia (ciclo futile).
-
1. Riassunto Esecutivo
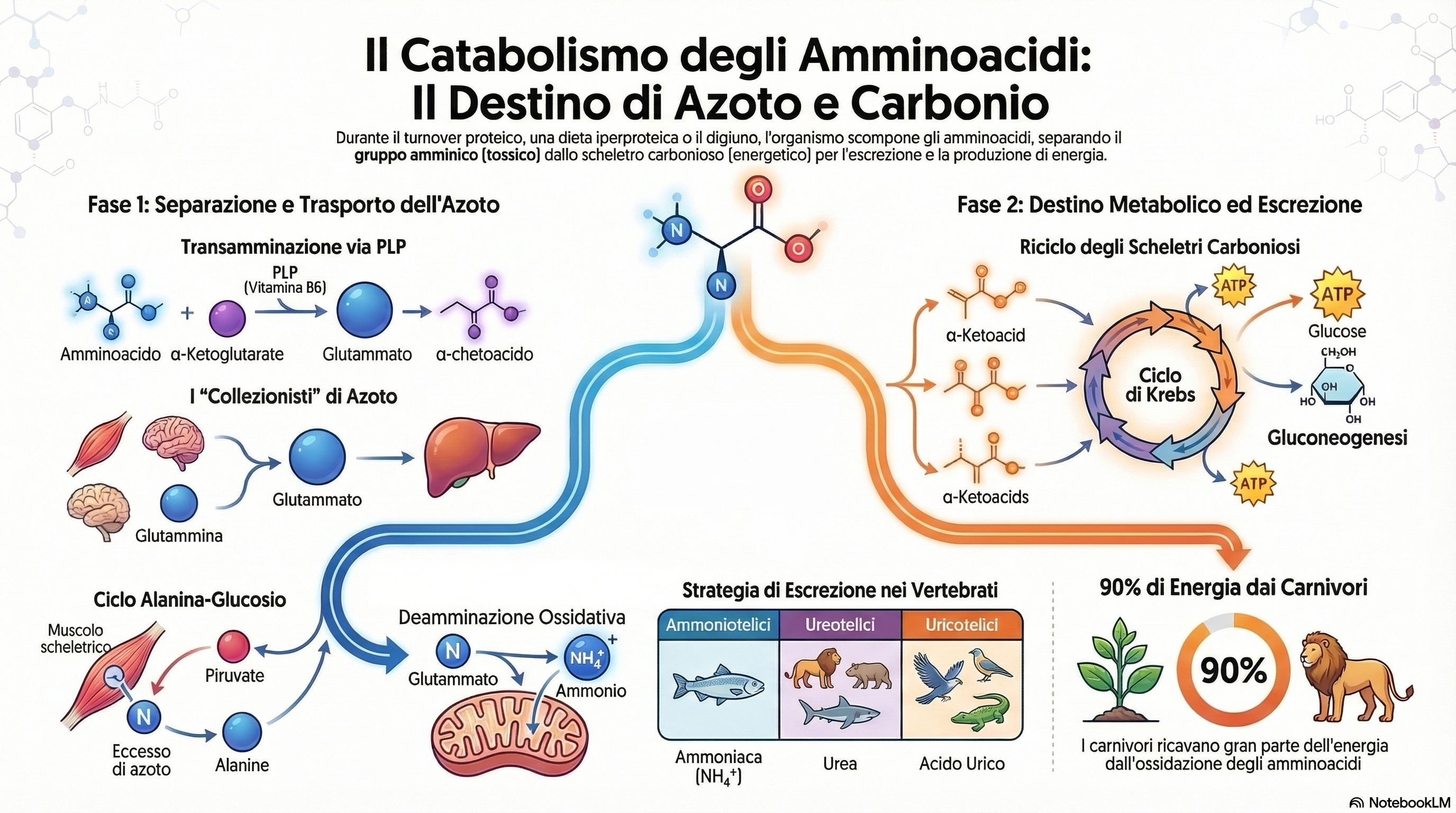
Gli amminoacidi rappresentano l’ultima classe di biomolecole che, attraverso la degradazione ossidativa, contribuiscono significativamente alla generazione di energia metabolica. Tuttavia, la loro importanza come combustibile varia drasticamente tra le specie: i carnivori possono ricavare fino al 90% del loro fabbisogno energetico dall’ossidazione degli amminoacidi subito dopo un pasto, mentre gli erbivori ne utilizzano solo una piccola percentuale e le piante li degradano quasi esclusivamente per produrre metaboliti biosintetici, mai per scopi energetici.
A differenza di carboidrati e grassi, gli amminoacidi non possono essere immagazzinati in forme di deposito (come glicogeno o trigliceridi); ogni molecola in eccesso rispetto alle necessità biosintetiche deve essere catabolizzata. Il processo richiede una tappa obbligata: la rimozione del gruppo -amminico per separarlo dallo “scheletro carbonioso”. Mentre l’azoto viene incanalato verso vie di escrezione per evitare la tossicità dell’ammoniaca libera, il residuo carbonioso viene ossidato a e nel ciclo dell’acido citrico o convertito in glucosio. Per uno studente di medicina veterinaria, comprendere queste vie è essenziale per interpretare patologie sistemiche, dal diabete non controllato alla gestione clinica delle disfunzioni pancreatiche.
-
1. Riassunto Esecutivo
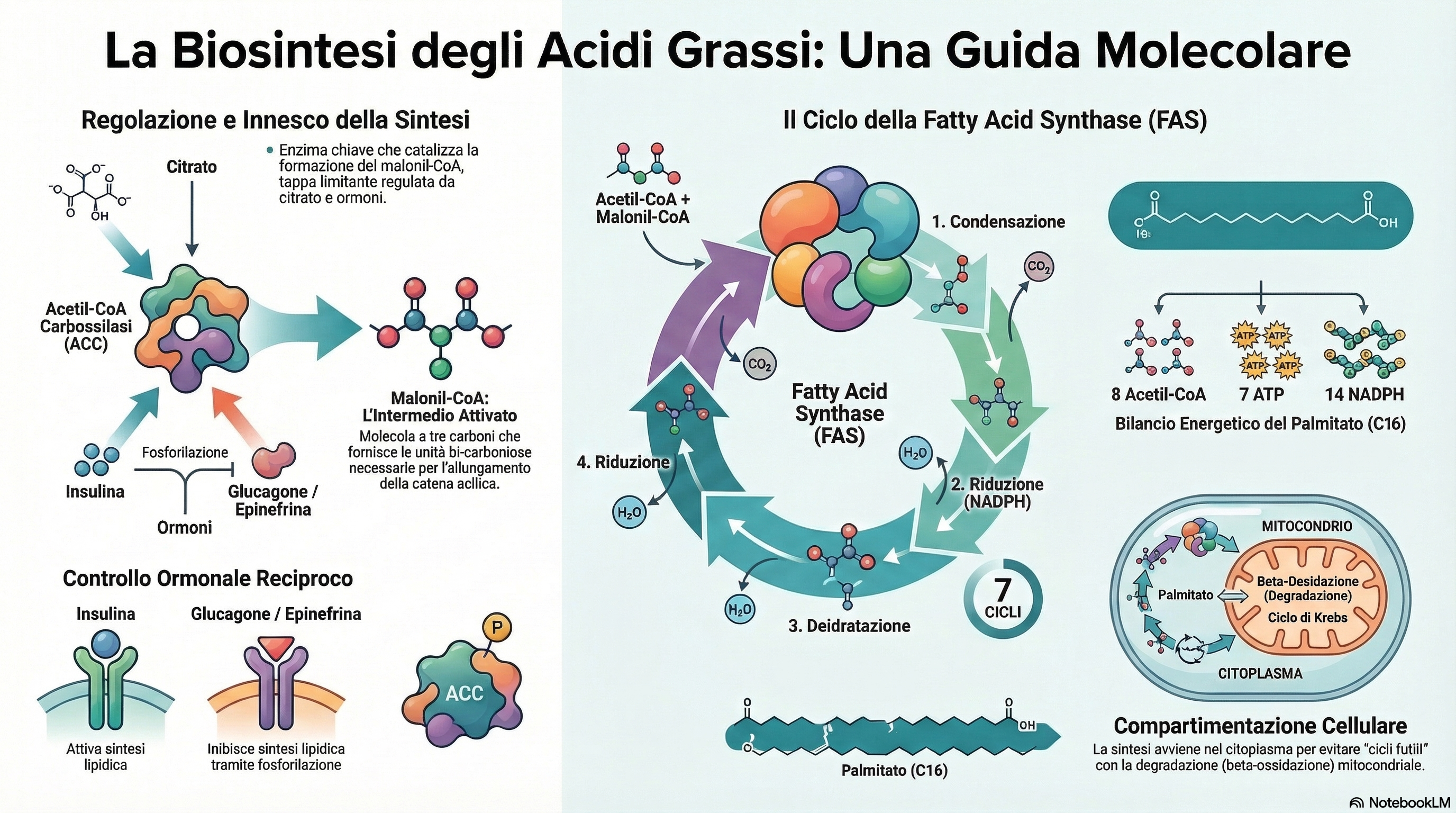
La biosintesi dei lipidi rappresenta un pilastro fondamentale del metabolismo cellulare, essenziale per la sopravvivenza di ogni organismo. I lipidi non sono soltanto la principale riserva di energia a lungo termine — con un contenuto energetico superiore a 38 kJ/g — ma costituiscono anche l’intelaiatura strutturale delle membrane biologiche e fungono da sofisticate molecole di segnalazione, come ormoni e messaggeri intracellulari. Per dare un’idea della loro rilevanza fisiologica, si consideri che un individuo di 70 kg può immagazzinare circa 15 kg di triacilgliceroli, una riserva sufficiente a sostenere il metabolismo basale per circa 12 settimane.
La cellula sintetizza grassi principalmente a partire da precursori idrosolubili semplici, come l’acetato. È cruciale comprendere che l’anabolismo (la sintesi) non è il semplice inverso del catabolismo (la degradazione). Le vie biosintetiche divergono da quelle degradative per poter superare tappe termodinamicamente irreversibili, permettendo alla cellula un controllo indipendente e coordinato dei due processi, evitando così cicli futili che sprecherebbero risorse preziose.
In quanto processo anabolico, la sintesi dei lipidi è endergonica, ovvero richiede un input di energia sotto forma di ATP, ed è riduttiva, necessitando di potere riducente fornito principalmente dal NADPH. In questa lezione analizzeremo come la cellula trasforma l’acetil-CoA in catene aciliche complesse, descrivendo la logica molecolare, i complessi enzimatici coinvolti e i raffinati meccanismi di regolazione che mantengono l’omeostasi lipidica.
-
1. Riassunto Esecutivo
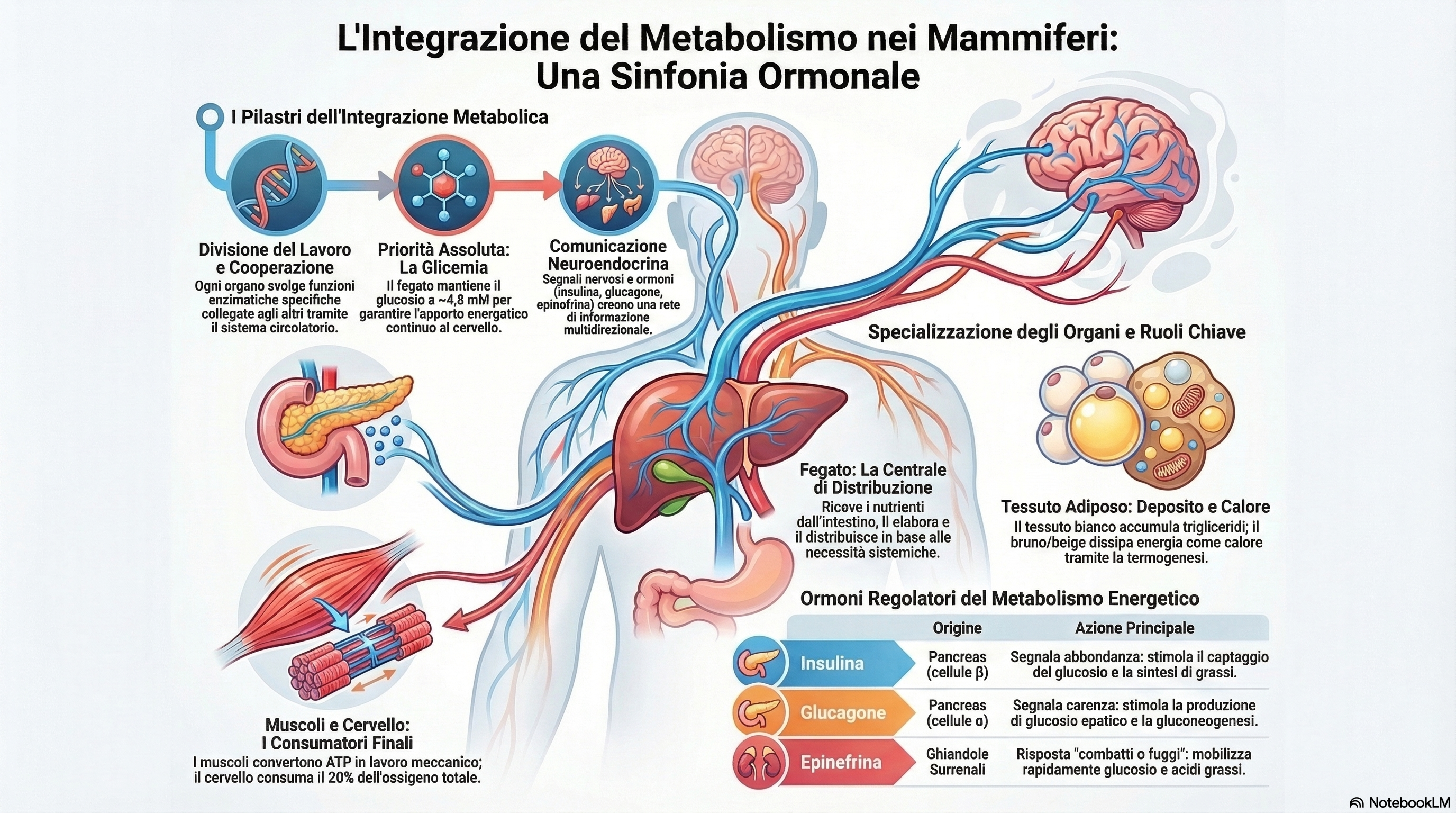
Il metabolismo non deve essere inteso semplicemente come un insieme di reazioni biochimiche isolate all’interno della singola cellula, bensì come un sistema integrato e coordinato a livello dell’intero organismo. Negli organismi multicellulari complessi, la sopravvivenza dipende dalla capacità di organi e tessuti specializzati di cooperare efficacemente. Questa cooperazione è orchestrata dal sistema neuroendocrino, che utilizza segnali ormonali e nervosi per ottimizzare l’allocazione delle risorse energetiche e dei precursori biosintetici in base alle necessità sistemiche.
In questo scenario, assistiamo a una precisa divisione del lavoro: il fegato agisce come centrale di elaborazione e distribuzione dei nutrienti; il tessuto adiposo funge da deposito energetico dinamico e organo endocrino; il muscolo rappresenta il motore meccanico; il cervello assume il ruolo di coordinatore supremo. Uno dei pilastri di questa integrazione è il mantenimento della glicemia (concentrazione di glucosio nel sangue) intorno al set-point di 4,5 mM. Tale parametro è vitale per il cervello, che dipende quasi esclusivamente dal glucosio per il proprio metabolismo energetico. Gli ormoni agiscono come messaggeri essenziali per mantenere l’omeostasi: l’insulina segnala l’abbondanza, mentre glucagone, epinefrina e cortisolo mediano le risposte alla carenza energetica o allo stress, garantendo che l’equilibrio metabolico sia preservato anche in condizioni critiche.
-
-
-